


Im interdisziplinären Forschungsverbund Matrix Evolution entwickeln Wissenschaftlerinnen aus unterschiedlichen Fachbereichen – der Medizinischen Hochschule Hannover (MHH) und der Leibniz Universität Hannover (LUH) – komplexe Biomaterialien, insbesondere für die regenerative Medizin und die Implantatforschung.
Das Niedersächsische Ministerium für Wissenschaft und Kultur fördert das Forschungsvorhaben für drei Jahre mit rund 1,5 Millionen Euro.
Im Fokus: Biomaterialien und regenerative Medizin
Biomaterialien spielen eine Schlüsselrolle bei Anwendungen der regenerativen Medizin. Die biophysikalischen und biochemischen Eigenschaften von Materialien erschaffen spezifische zelluläre Milieus, die maßgeblich Zellverhalten und -funktion beeinflussen. Eine breite Palette an natürlichen und synthetischen Stoffen wird zurzeit im Bereich der regenerativen Medizin (Tissue Engineering) und Implantatforschung eingesetzt oder für die Anwendung erforscht. Obwohl diese Biomaterialien wichtige Anforderungen wie Biokompatibilität, Abbaubarkeit oder mechanische Stabilität bereits erfüllen, stellen sie letztendlich häufig stark vereinfachte Modelle der extrazellulären Matrix (EZM) dar. Die hierarchisch aufgebaute, stark kompartimentalisierte und dynamische Komplexität der realen EZM wird durch die Verwendung unstrukturierter Biomaterialien längst nicht erreicht. Die In-vitro-Modelle aus heute gängigen Biomaterialien bleiben damit stark vereinfacht und können die volle biologische Funktion von Gewebe nicht nachbilden. Daher werden dringend Biomaterialien benötigt, die wie die natürliche Matrix eine hierarchische Strukturierung und Komplexität aufweisen, und den Aufbau von definierten Architekturen von der Nano- bis hin zur 3D-Makroebene ermöglichen. Die natürliche EZM ist nicht nur hochstrukturiert, sondern auch hochdynamisch und wird in physiologischen Prozessen umgebaut und angepasst. Daher soll im Projekt Matrix Evolution auch dieser dynamische Aspekt nachgebildet werden, indem bioresponsive und temporal-schaltbare Elemente in die Biomaterialien eingeführt werden. Neue, bioinspirierte Matrixmoleküle und -materialien können zu einer Evolution der Matrix in der Gewebemodellierung führen, mit erheblichen Vorteilen für alle Bereiche der regenerativen Medizin und der klinischen Forschung.
MatrixNische | Prof. Dr. Cornelia Lee-Thedieck
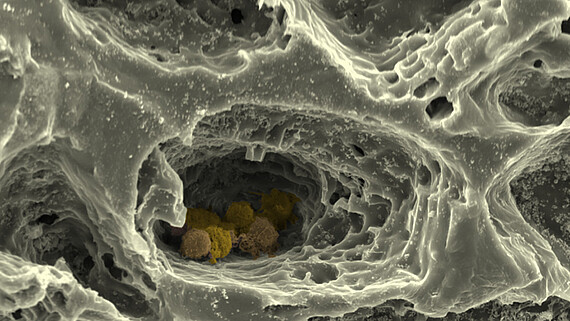
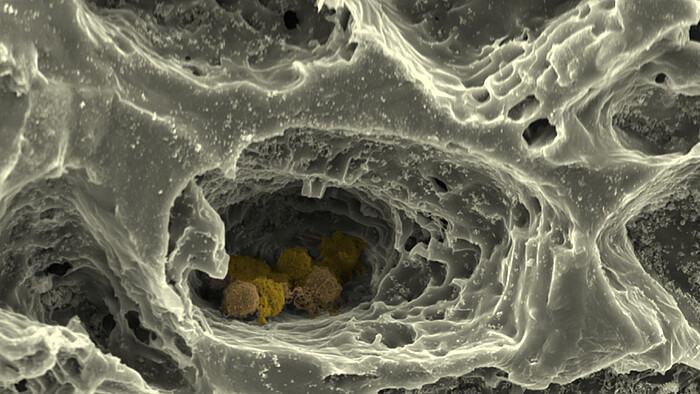
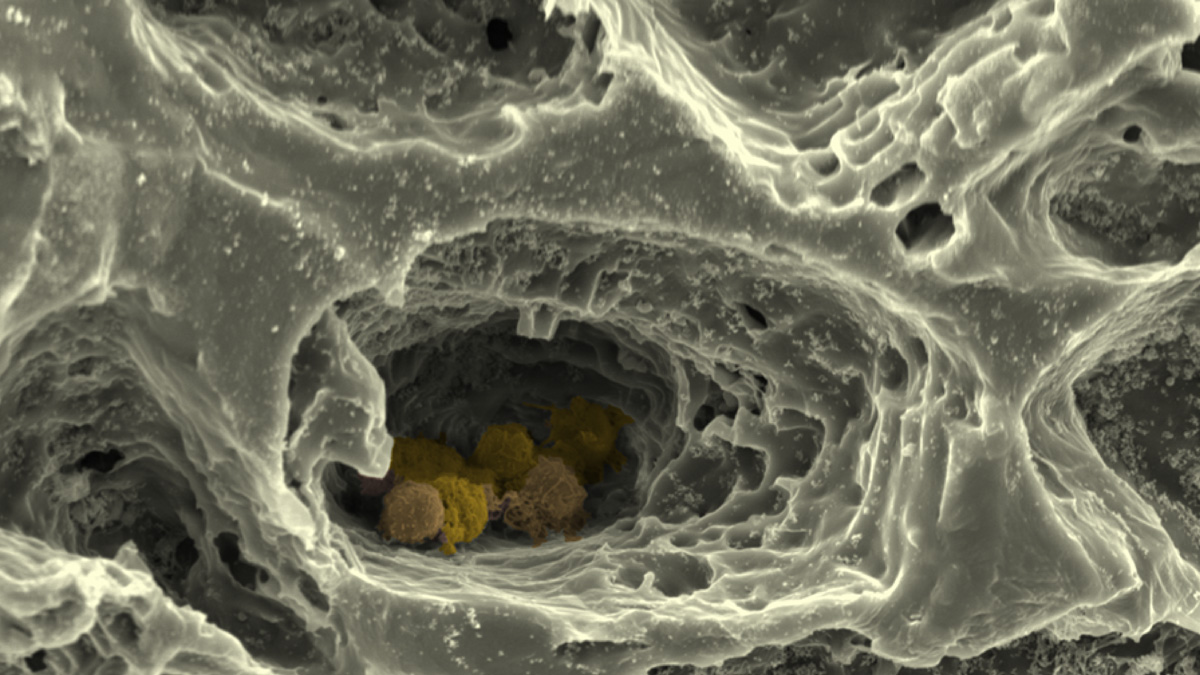
Am Institut für Zellbiologie und Biophysik ahmen wir in der Abteilung Zellbiologie im Teilprojekt „MatrixNische“ die EZM des Knochenmarks und die Struktur des umgebenden Knochens durch Kombination verschiedener Matrixmoleküle in einem hierarchisch organisierten, biomimetischen Biomaterial nach, das durch 3D-Druck, Elektrospinnen und den Quervernetzung von Polymeren zu Hydrogelen erzeugt wird. Diese maßgeschneiderte Matrix erlaubt es uns, den kombinierten Einfluss unterschiedlicher Parameter – wie Nanostruktur, Makrostruktur, Steifigkeit und Porosität – auf Stammzellen des Knochenmarks mit Hilfe hochauflösender Licht- und Rasterkraftmikroskopie, Einzelzellkraftspektroskopie sowie moderner biochemischer, zell- und molekularbiologischer Methoden zu untersuchen. Die hierarchisch strukturierte Matrix verwenden wir in "MatrixNische" weiter als Gerüststruktur für ein aus multiplen Zelltypen aufgebautes, biomimetisches in vitro-Modell der Stammzellnische im Knochenmark , was uns die Analyse zellulärer Wechselwirkungen in Abhängigkeit von Matrixeigenschaften in der Nische erlaubt.
MatrixBlocks | Prof. Dr. Marie Weinhart



Im Institut für Physikalische Chemie und Elektrochemie, Abteilung Polymere und Biomaterialien, synthetisieren wir im Rahmen des Teilprojekts „MatrixBlocks“ zellkompatible Blockcopolymere mit intrinsisch zelladhäsiven Eigenschaften. Die funktionalen Polymere sind in ihrer chemischen Zusammensetzung und Architektur so designt, dass sich reversibel verknüpfte Hydrogele mit einstellbaren mechanischen Eigenschaften erzeugen lassen. Gleichzeitig ermöglicht die Blockcopolymer-Struktur eine Selbst-Assemblierung auf elektrogesponnenen Netzwerkfasern mit nachfolgender kovalenter Anbindung, um in Kombination mit den reversibel gelierenden Gelen zelladhäsive, hierarchisch strukturierte synthetische Matrizes für Säugerzellen zu erzeugen. Mit Hilfe rheologischer Messungen, einer Quarz-Kristall-Microwaage und Lebend-Zell-Mikroskopie untersuchen wir die Bioabbaubarkeit und Modellierbarkeit der Matrix in An- und Abwesenheit von Zellen, um sie dann für spezifische Anwendungen im Forschungsverbund zu optimieren.
MatrixSynBio | Prof. Dr. Selin Kara



In der Arbeitsgruppe Design von Biomaterialien mit Biotechnologie, nähern wir uns in MatrixSynBio der Aufgabe, eine hierarchisch strukturierte und dynamische extrazelluläre Matrix zu schaffen, von der Seite der Protein-Biomaterialien. Unser Projektmodul ist am Institut für Technische Chemie angesiedelt. Hier nutzen wir unsere Expertise in der Bioverfahrenstechnik, um rekombinante Segmente der extrazellulären Matrix durch mikrobielle Fermentation herzustellen. Dadurch können wir Biomaterialien in gleichbleibender Qualität produzieren und die Risiken der herkömmlichen Beschaffung aus tierischen Produkten verringern. Die anschließende Erzeugung hierarchischer Strukturen wird durch chemische Modifizierung der EZM-Segmente erreicht, was die Weiterverarbeitung des Materials zu gewünschten Geometrien durch Elektrospinnen oder Bioprinting ermöglicht. Die rekombinante Technologie kann aber auch eingesetzt werden, um bestimmte Aspekte der EZM in der rekombinanten Matrix nachzubilden, wie z. B. die Fähigkeit zur Wachstumsfaktorbindung und Zelladhäsion sowie die self-assembly der Proteine zu höheren Strukturen.
MatrixSense | PD Dr. Antonina Lavrentieva


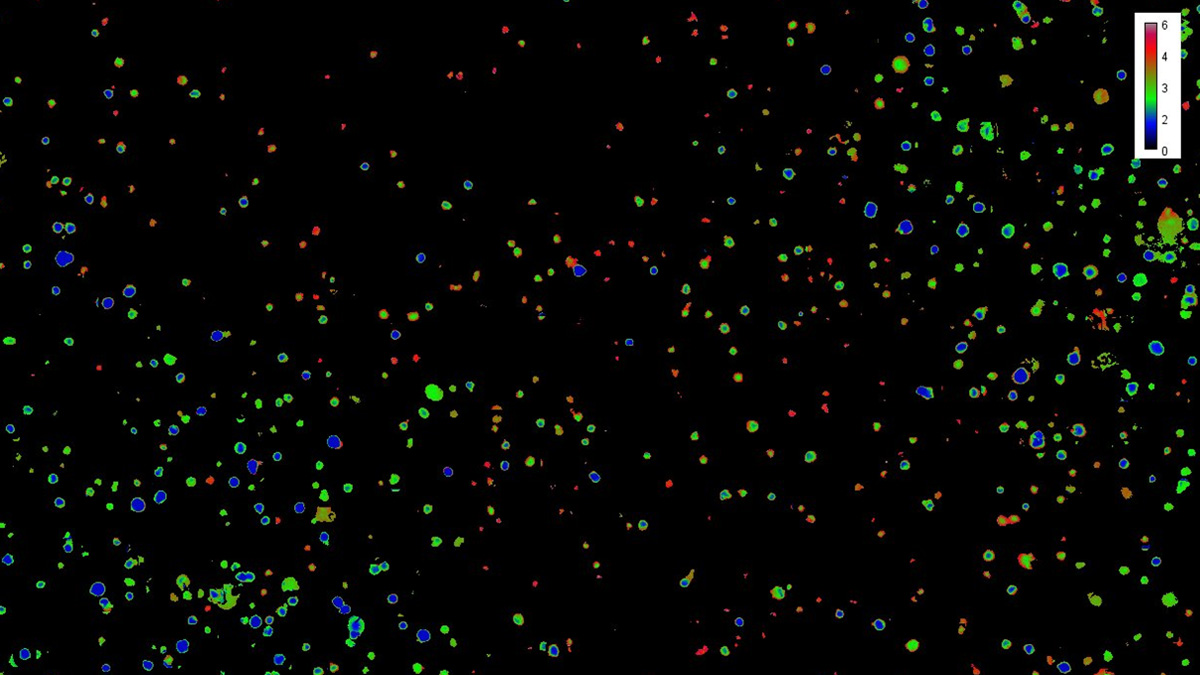
Der Einfluss von hierarchischen, synthetischen Matrizes auf Zellen wird normalerweise durch Endpunktanalysen wie Zellviabilitätsfärbungen und –assays, sowie Immunhistochemie untersucht. 3D-Matrix-basierte Zellkonstrukte stellen jedoch ein offenes dynamisches System dar, das hochempfindlich auf eine Fülle von Faktoren und Stimuli reagiert, die Zellen in intrazelluläre Signale umwandeln. Im Teilprojekt „MatrixSense“, das am Institut für Technische Chemie, AG Zellkulturtechnologie, durchgeführt wird, stecken wir uns diese Hauptziele: die Integration von genetisch kodierter Biosensoren in relevanten Zelltypen, Charakterisierung von den Reporter-Zellen in 2D und 3D Zellkultursystemen und die Online-Evaluierung der räumlich-zeitlichen Zellantwort auf Einzelzellebene in synthetisierten Matrizen. Ferner vergleichen wir Reporterzellreaktionen mit nicht-invasiv gemessenen in situ Parametern (e.g. O₂, pH, CO₂). Genetisch kodierte Biosensoren auf der Basis von Fluoreszenzproteinen ermöglichen die Echtzeitüberwachung der Molekulardynamik in Raum und Zeit, die für die Evaluation von hergestellten Biomaterialien entscheidend ist. Wir intergrieren Hypoxie-, Apoptose-, Yes-assoziiertes Protein YAP, Actin-, pH- und Vinculin-Sensoren in MSZ und Endothelzellen. Für Überwachung von Zellsignalen verwenden wir ein neuartiges Live-Cell-Analysesystem mit hochauflösender Fluoreszenzbildgebung, das es ermöglicht, komplexe biologische Veränderungen in Echtzeit zu beobachten und zu quantifizieren. Reporterzellen werden direkt auf die synthetisierten hierarchischen Matrizen angewendet, Zellreaktionen werden überwacht und die Korrelation zwischen Matrixstruktur und z. B. Zellskelettstruktur, hypoxischer Reaktion, Translokation von YAP und Expression von Vinculin werden untersucht.
MatrixModel | Prof. Dr. Sophia Rudorf

Die Zusammenführung experimenteller Erkenntnisse in quantitativen Modellen dient nicht nur einem tieferen Prozessverständnis, sondern kann auch den Zugriff auf experimentell unzugängliche Informationen ermöglichen. In der Abteilung Computational Biology des Instituts für Zellbiologie und Biophysik bringen wir unsere Erfahrung in der theoretischen Beschreibung und Simulation biomolekularer Prozesse in das Teilprojekt "MatrixModel" ein. Wir nutzen die experimentellen Ergebnisse aus den Teilprojekten MatrixSynBio, MatrixBlock, MatrixSense und MatrixNische, um in-silico-Modelle der bioinspirierten Matrizes zu entwickeln. Dabei berücksichtigen wir insbesondere die hierarchische Struktur der Matrix und die physikalisch-biologischen Wechselwirkungen zwischen der Matrix und verschiedenen Zelltypen. Die Modelle werden in MatrixModel und den anderen Teilprojekten im Rahmen von Prädiktions-Validierungs-Zyklen getestet und für die Optimierungen der Matrizes eingesetzt. So soll eine noch zielgerichtetere Entwicklung der Materialien ermöglicht werden.
Überdies unterstützen wir die Synthese von EZM-Proteinen in Mikroorganismen in Teilprojekt MatrixSynBio mithilfe unserer Expertise in der Optimierung genetischer Sequenzen.
MatrixImplant | Prof. Dr. Meike Stiesch
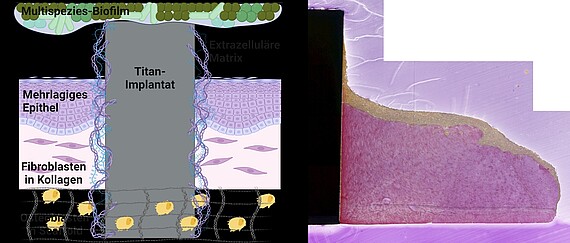
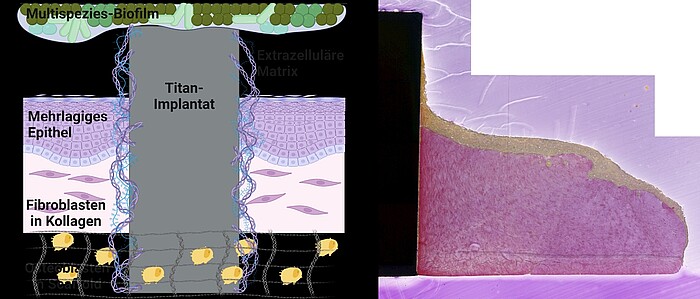
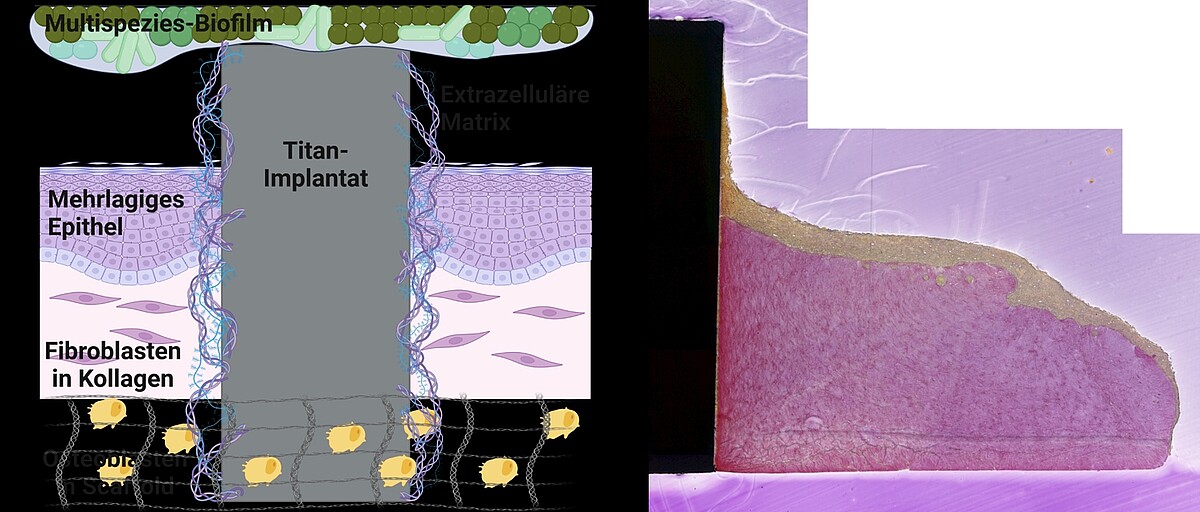
In „MatrixImplant“ erforschen wir den Einfluss der extrazellulären Matrix auf die Entstehung schwer behandelbarer Implantat-assoziierter Infektionen in der Klinik für Zahnärztliche Prothetik und Biomedizinische Werkstoffkunde der Medizinischen Hochschule Hannover. Dafür integrieren wir die strukturierte, rekombinante Matrix in das komplexe 3D-implant-tissue-oral-bacterial-biofilm (INTERbACT)-Modell. Das Modell besteht aus einer artifiziellen, mehrschichtigen Mukosa mit integriertem Implantat in Co-Kultur mit einem oralen Multispezies-Biofilm, und bildet somit alle relevanten Faktoren des periimplantären Systems ab. Durch die rekombinante Matrix hervorgerufene Veränderungen des Implantatmaterials auf physikalischer und chemischer Ebene untersuchen wir mittels Rasterkraft- und Rasterelektronenmikroskopie sowie Kontaktwinkelmessung. Der Einfluss der Matrix auf die Vitalität und Integration periimplantärer humaner Zellen im INTERbACT-Modell wird von uns fluoreszenzmikroskopisch, histologisch und molekularbiologisch analysiert. Das Modell erweitern wir dabei um Knochengewebe, um den Einfluss der extrazellulären Matrix auch auf die knöcherne Einheilung zu untersuchen. Die Ergebnisse der Matrix-Material- und Matrix-Zell-Interaktionen nutzen wir, um die Rolle der Matrix im Infektionsgeschehen zu analysieren und so neue Ansätze zur Entwicklung innovativer infektionsresistenter Biomaterialien zu entwickeln.
Förderung und Kooperation
Matrix Evolution wird gefördert mit Mitteln aus zukunft.niedersachsen, ein Förderprogramm des Niedersächsischen Ministeriums für Wissenschaft und Kultur und der VolkswagenStiftung.



Medizinische Hochschule Hannover



Leibniz Universität Hannover



Agenda zukunft.niedersachsen
Sprecherin Matrix Evolution


30419 Hannover




